信頼性保証
基本理念と方針
生活者の方々の安心と満足を得るためには、全従業員が同じ理念に基づき、真摯に業務に取り組むことが必要です。当社では、経営理念のもとに信頼性保証基本理念を定めて、信頼性に関する考え方を徹底しています。
この基本理念を実現するためには、
- 常に生活者の皆様からのご意見を真摯に受け止め、品質向上・安全管理に活かすこと
- 科学技術の進歩や製品の多様化に伴い、信頼性保証のための手法も進歩・変化するため、最新の知識を身につけること
- 多くの部署が連携して業務を進めるために、関係する部署間の連携体制を整え責任体制を明確にして、常に組織を活性化しておくこと
が大切と考えています。
そのため、これら1~3を信頼性保証業務の基本方針として定め、常に信頼性保証体制をより良いものに整備・強化するよう努めています。
信頼性保証基本理念
生活者の視点から、当社製品等の「有効性」、「安全性」の確保と「品質」の向上に努め、信頼、即ち「安心」と「満足」を得る。そのために責任を持って行動する。
信頼性保証基本方針
- 姿勢:生活者の意見に耳を傾け、その期待に応える。
- 技術水準:世界的視野に立ち、最高の水準を求め続ける。
- マネジメント:信頼性が保証されるようマネジメントに万全を期する。
品質方針
生活者の信頼・安心・満足が得られる、品質、有効性及び安全性の確かな製品を供給し続ける。
信頼性保証体制
創業の精神に則り、全ての生活者の方々に信頼していただける製品・情報・サービスを提供することが、大正製薬グループの社会的責任であると考えています。この責任を果たすためには、まず「製品」に関する研究開発・製造・販売など全ての業務を、関連した法規制を遵守し、製品の有効性・安全性・品質の信頼性確保を最優先で実施しなければなりません。さらに、これらの業務が生活者の方々から信頼をいただけるものであることを、生活者視点でしっかりと確認することが重要です。これに取り組むことが「信頼性保証業務」です。
大正製薬では、研究開発・製造・販売などのラインから独立したQA(Quality Assurance:信頼性保証)本部が中心となって、「信頼性保証業務」を推進する体制の維持・向上を図りながら、生活者の方々から高い信頼をいただける製品・情報・サービスを提供することを目指して日々業務を推進しています。
大正製薬ホールディングスと大正製薬の信頼性保証組織
| 部署名 | 事業内容 | |
|---|---|---|
| 大正製薬ホールディングス | QA統括室 | 国内外の大正製薬グループ各社の製品の品質保証と安全管理 |
| 大正製薬QA本部 | 品質保証部 | 医薬品、医薬部外品、化粧品、医療機器及び食品等の品質保証 |
| 医薬安全管理部 | 医療用医薬品及び治験薬の安全管理 | |
| 市販後調査部 | 医療用医薬品の製造販売後調査等における信頼性保証業務 | |
| セルフメディケーション安全管理部 | 要指導・一般用医薬品、医薬部外品、化粧品、食品及び治験薬等の安全管理、要指導医薬品の製造販売後調査 | |
| 治験監査室 | 治験のGCP※監査、臨床試験の信頼性保証 | |
| 試験保証室 | 非臨床試験の信頼性保証、治験薬の品質保証 | |
| QA推進室 | 製造販売業業態管理、研究開発から製造販売後の信頼性保証の推進、QA本部の運営管理 | |
- ※ GCP(Good Clinical Practice):臨床試験の実施基準
QA本部の役割
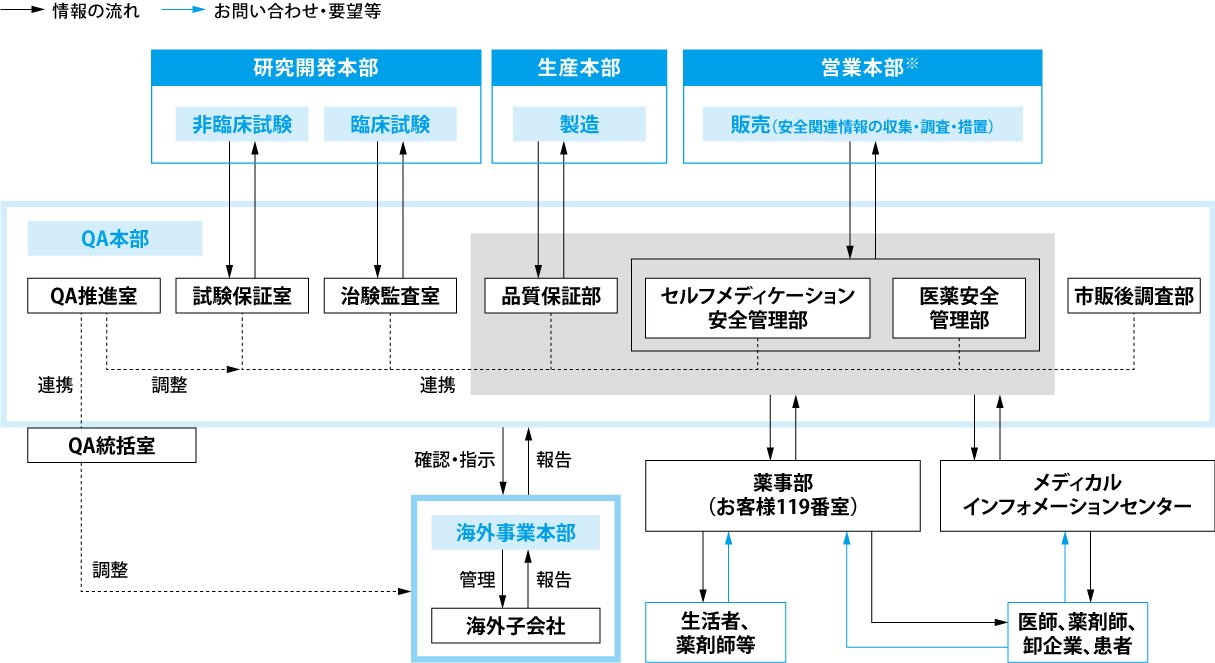
研究開発段階では、有効性や安全性を評価する各種試験が適切な方法で実施し、高品質な製品を製造する方法が開発され、それらの記録が信頼性の確保された形で保存されていることが大切です。試験保証室及び治験監査室が、これらの信頼性保証業務を担当しています。製造販売段階では、適切な設備において定められた手順で製品が製造・出荷され、さらに市場においても品質が確保された製品が販売されていることを、品質保証部が常に監視しています。また、製品の正しい使用方法や安全性情報を生活者や医療関係者の皆様に速やかにお届けするため、有効性及び安全性に関する情報を収集・調査して評価し、適切な措置を講じるための業務を行います。大正製薬では製品特性や販売形態の違いを考慮し、医療用医薬品を担当する医薬安全管理部及び市販後調査部と要指導・一般用医薬品等を担当するセルフメディケーション安全管理部という専門組織を設置し、各々の業務を実行しています。
このように信頼性保証業務は多くの部署が協力して行う必要がありますが、業務分担と責任を明確化した連携体制を作り、運営する役割もQA本部が担当しています。
大正製薬QA本部の運営体制
国内外グループ会社における取り組み
大正製薬では、国内外のグループ各社における品質保証・安全管理業務を高いレベルで推進するため、本社を中心とした管理体制を構築しています。また、グローバル品質保証システムの構築に積極的に取り組んでいます。加えて、海外では、医薬品をより安全に、より安心してお使いいただくため、安全性の評価・見直しを適切に行い、安全確保措置を的確に実施していけるよう、本社とグループ各社の連携を強化したファーマコビジランス体制を構築しています。
各国の法規制を遵守し、大正製薬グループの基本理念を共有して、海外の皆様にも信頼していただける製品・情報・サービスを提供するよう取り組んでいます。
品質保証・製造販売後安全管理業務に関する従業員教育
当社では、GQP省令※1およびGVP省令※2に基づき、品質管理業務や製造販売後安全管理に従事する者への教育に関する手順を定め、教育を実施しています。
品質保証責任者による責任のもと、品質管理業務に従事する者を対象に、日常の業務の適切な遂行に必要な基礎知識習得のための教育や、実地監査の訓練(OJT)、社外講師による教育などを継続的に実施しています。
一方、セルフメディケーション安全管理責任者や医薬安全管理責任者の責任のもと、製造販売後安全管理業務に従事する者を対象に、業務遂行能力を確保して、安全確保業務を適正に実施し信頼性を確保するための教育を継続的に実施しています。なお、新任者は導入教育実施後に理解度を確認するためのテストを行い、テストに合格した後、業務に従事するようにしています。
また、製薬企業の使命として、薬害防止や品質管理・製造販売後安全管理のための教育を実施する必要があるとの考えから、全従業員に向けた教育の機会を毎年設けております。これにより、全従業員の意識の向上を図っています。
- ※1 GQP:Good Quality Practiceの略。医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準に関する省令
- ※2 GVP:Good Vigilance Practiceの略。医薬品、医薬部外品、化粧品、医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令
臨床試験(治験)の実施における信頼性確保
医薬品医療機器法、ICH-GCP※、臨床試験実施国のGCPなど、関連法規制に基づき、当社の臨床試験(治験)の実施体制を定めています。このなかで、被験者の人権保護を最優先とする方針を明示するとともに、各責任者や委員会などを規定し、責任と役割を明確にして臨床試験(治験)のデータの信頼性確保に努めています。
- ※ ICH-GCP:医薬品規制調和国際会議(ICH)で定められた、医薬品の臨床試験の実施基準(GCP)